3月29日,国家药监局发布《河北宝塔医疗器械有限公司对医用口罩、医用防护口罩主动召回的公告》以及《河北宝塔医疗器械有限公司对医用外科口罩主动召回的公告》。
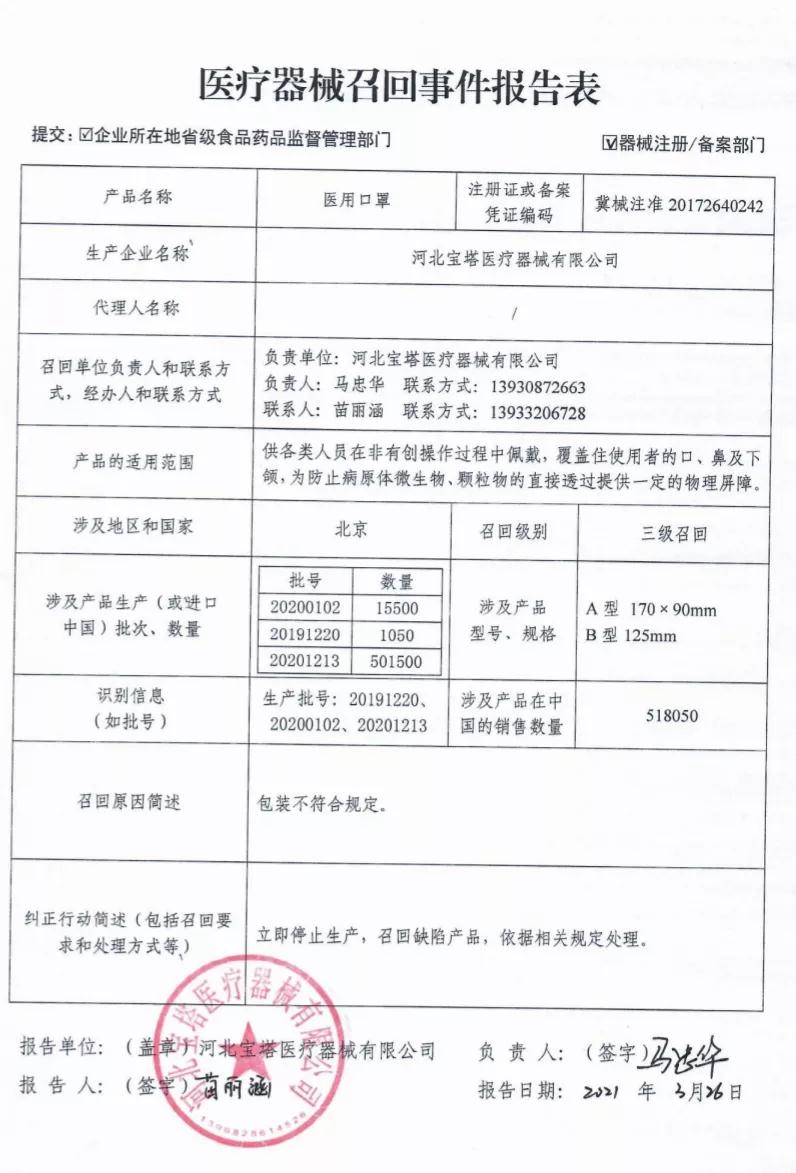
上述公告显示,河北宝塔医疗器械有限公司报告:由于包装不符合规定,河北宝塔医疗器械有限公司对其生产的医用口罩(注册号:冀械注准20172640242)和医用防护口罩(注册号:冀械注准20172640241)进行主动召回,召回级别为三级召回。
涉及产品在国内销售数量为518050。
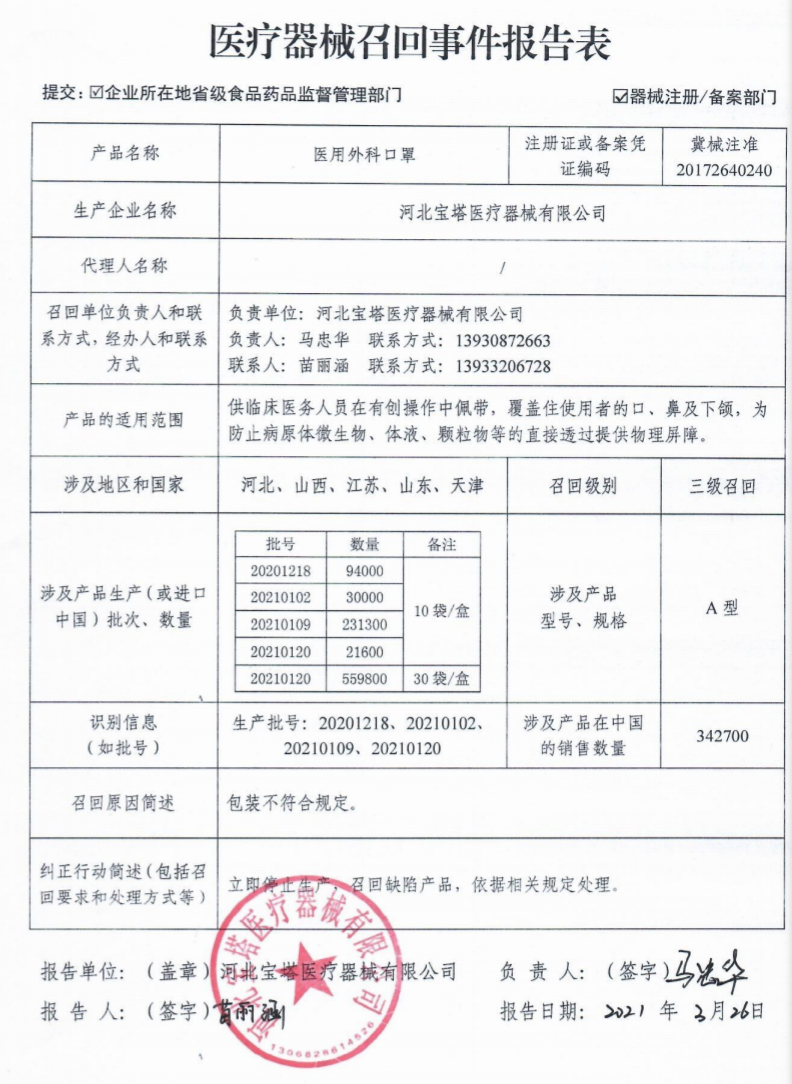
河北宝塔医疗器械有限公司报告:由于包装不符合规定,河北宝塔医疗器械有限公司对其生产的医用外科口罩(注册号:冀械注准20172640240)进行主动召回,召回级别为三级召回。
涉及产品在国内销售数量为342700。
知名械企产品召回
同时,国家药监局还发布了《飞利浦金科威(深圳)实业有限公司对病人监护仪主动召回》的公告。
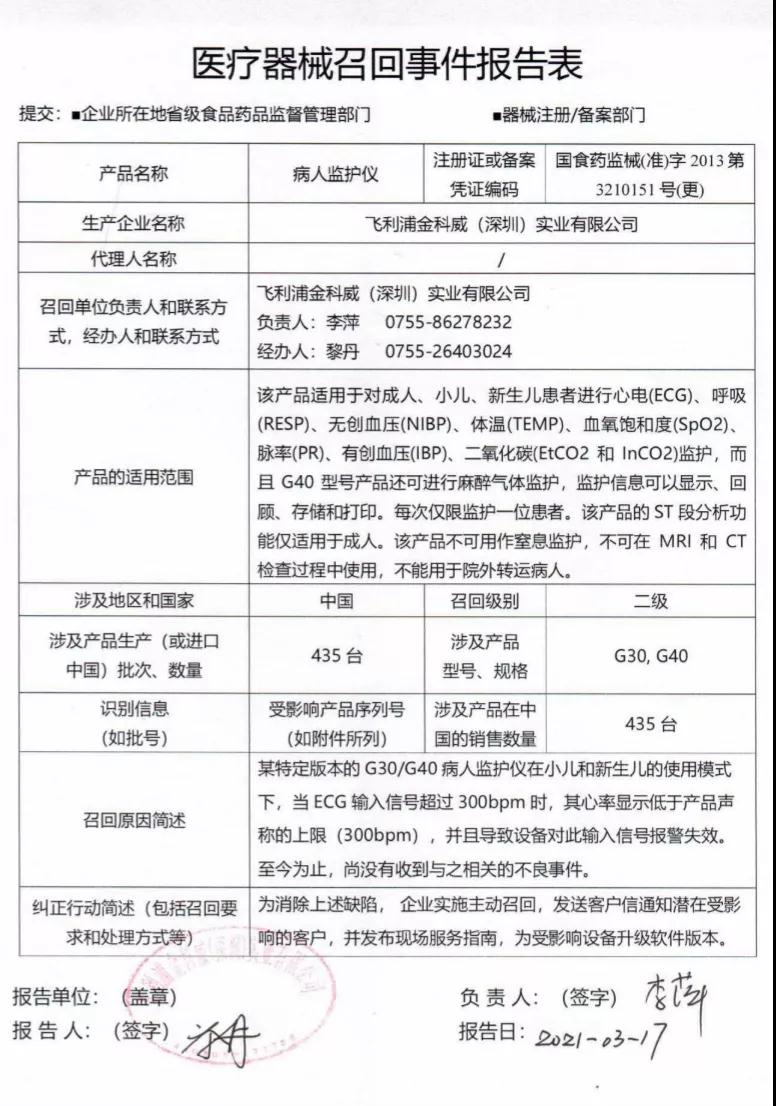
上述公告显示,飞利浦金科威(深圳)实业有限公司报告,G30/G40病人监护仪在小儿和新生儿模式下使用,当ECG输入信号超过300bmp时,其心率显示低于产品声称的上限(300bmp),并且导致设备对此输入信号报警失效。飞利浦金科威(深圳)实业有限公司对其生产的病人监护仪主动召回。召回级别为二级
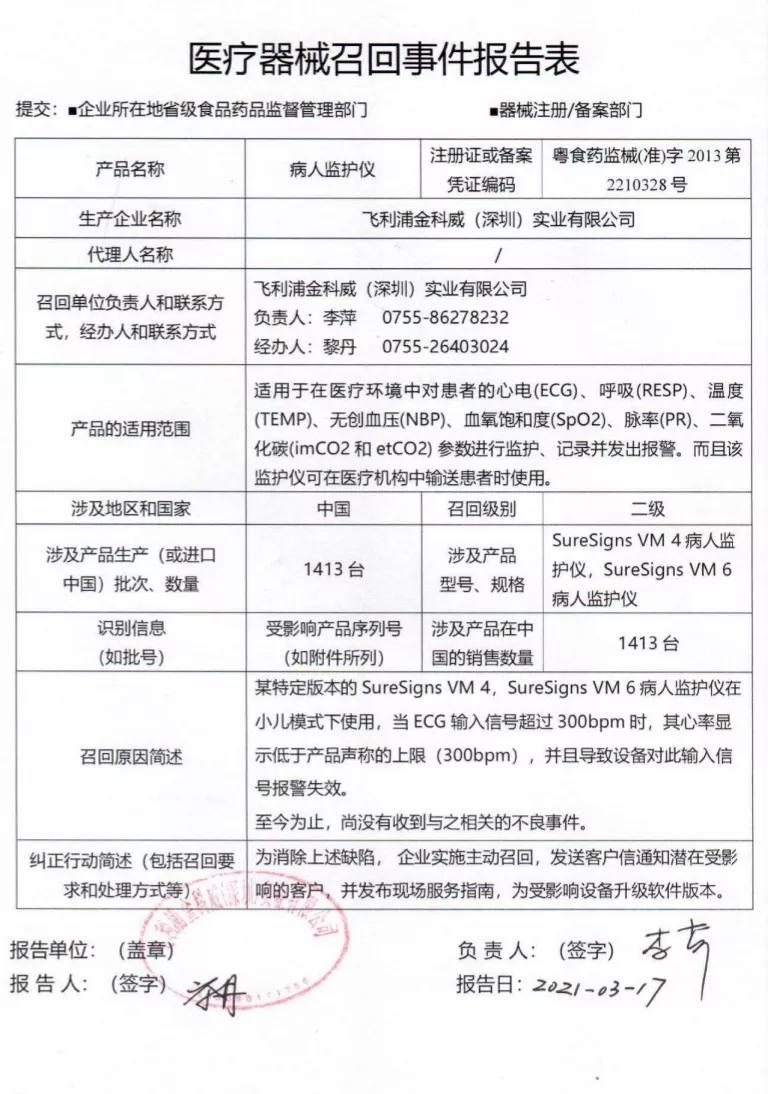
SureSigns VM 4,SureSigns VM 6病人监护仪在小儿模式下使用,当ECG输入信号超过300bmp时,其心率显示低于产品声称的上限(300bmp),并且导致设备对此输入信号报警失效。飞利浦金科威(深圳)实业有限公司对其生产的病人监护仪主动召回。召回级别为二级。

Copyright 2020 yaoxie.com 互联网药品信息服务资格证书(闽)-经营性-2019-0023 互联网药品交易服务资格证书-国A20150004
闽ICP备14018699号-4 增值电信业务经营许可证 闽B2-20140006 闽公网安备35030502000131号 营业执照:91350300056126227U
医疗器械网络交易服务第三方平台备案凭证 备案编号:(闽)网械平台备字(2018)第00001号
药品网络交易第三方平台备案凭证 (闽)网药平台备字 (2023) 第000004-000号